Вплив вакуумної терапії на морфологічні зміни м'яких тканин ранових дефектів у хворих із синдромом діабетичної стопи

На 10 добу ексудативно-деструктивні прояви зберігалися із слабовираженою тенденцією до згасання. На цьому терміні запальний інфільтрат складався переважно із полінуклеарних лейкоцитів та макрофагів, поширювався на всю товщу дерми, проникаючи в субдермальні ділянки та м’язову тканину. Подекуди спостерігали абсцедування. Мікроциркуляторні розлади у вигляді повнокров’я дилатованих судин, стазу та… Читати ще >
Вплив вакуумної терапії на морфологічні зміни м'яких тканин ранових дефектів у хворих із синдромом діабетичної стопи (реферат, курсова, диплом, контрольна)
Анотація
У статті наведено результати вивчення динаміки морфологічних змін м’яких тканин ранових дефектів у хворих із синдромом діабетичної стопи на тлі вакуумної терапії. Встановлено, що вакуумна терапія значно поліпшує мікроциркуляцію в ділянці ран, зменшує прояви запальних та деструктивних змін, пришвидшує організацію екстрацелюлярного матриксу, оптимізуючи таким чином регенераторний процес та формування якісної грануляційної тканини. Вона стимулює процеси регенерації та дозволяє скоротити терміни підготовки ран до пластичного закриття в середньому на 5 днів.
Ключові слова: синдром діабетичної стопи, вакуумна терапія ран, морфологічні зміни.
Лікування гострих та хронічних ранових дефектів у хворих із синдромом діабетичної стопи (СДС) не втрачає своєї актуальності. Це зумовлене тим, що наявність тривалого і неконтрольованого перебігу цукрового діабету спотворює перебіг ранового процесу та сповільнює процеси регенерації. В основі порушення регенераторних процесів лежать діабетична мікро-, макроангіопатія, діабетична периферична нейропатія, порушення всіх видів обміну в організмі, розвиток ацидозу, гіпоксії та метаболічної інтоксикації. Тривале порушення трофіки тканин у хворих із СДС спричиняє не лише метаболічні зміни, але і призводить до розвитку грубих морфологічних змін у тканинах, які можуть мати самостійне значення в розвитку та перебігу гнійнонекротичних уражень [1−4].
На сьогодні продовжується пошук нових, ефективних методів місцевого лікування ранових дефектів у хворих із СДС. Одним з нових і сучасних методів є вакуумна терапія, яку починають все ширше використовувати у вищезазначених хворих. Позитивний вплив вакуум-терапії на перебіг ранового процесу визнали багато авторів [5−7]. Однак її вплив на морфологічні зміни тканин вивчено недостатньо і потребують свого подальшого дослідження [8, 9].
Метою дослідження було вивчити вплив вакуумної терапії на особливості морфологічних змін тканин гострих та хронічних ран нижніх кінцівок у хворих із синдромом діабетичної стопи.
Всього обстежено 38 хворих із СДС, які перебували на стаціонарному лікуванні в клініці загальної хірургії ДВНЗ «Тернопільський державний медичний університет імені І.Я. Горбачевського» протягом 2014;2015 року. Чоловіків було 25, жінок — 13 віком від 46 до 58 років. Гострі рани діагностовано у 21 пацієнта, хронічні рани та трофічні виразки — у 17 хворих. Забір морфологічного матеріалу проводили інтраопераційно та під час перев’язок таким чином, щоб на одному рівні дослідити шкіру з підшкірною основою, фасції, сухожилки, м’язи.
Вивчено особливості динаміки патоморфологічних змін тканин ранових дефектів у 28 хворих із СДС (основна група), в яких використано вакуумну терапію ран. Досліджено 142 гістологічних препарати, які виготовили з біопсійного матеріалу, отриманого при виконанні первинного хірургічного втручання, та на 3, 5, 10, 15 доби вакуумної терапії ран. Групою порівняння слугували 52 препарати, виготовлені з біопсійного матеріалу, взятого в аналогічні терміни у 10 пацієнтів, у яких вакуум-терапію в лікуванні ран не використовували. Препарати виготовляли за стандартними методиками і забарвлювали за допомогою гематоксиліну та еозину, з подальшим дослідженням за допомогою світлової мікроскопії.
При мікроскопічному дослідженні м’яких тканин нижніх кінцівок із ділянок ран пацієнтів групи порівняння протягом перших 3 діб спостерігали гострі некротично-запальні зміни. Відмічали виражений набряк тканин, дезорганізований екстрацелюлярний матрикс, відсутність фібро-бластоподібних клітин. Густа інфільтрація полінуклеарами подекуди поєднувалася із чисельними колоніями бактерій. На поверхні ранового дефекту знаходилися гнійно-фібринозні маси та тканинний детрит. Епідерміс на краях рани зазнавав дистрофічних змін — епітелій вакуолізовувався і злущувався. Подекуди він був частково або повністю відсутній (рис. 1).
Дерма та елементи пухкої сполучної тканини знаходилися в стані деструкції з утворенням мікроабсцесів. Окрім цього, спостерігали виражені розлади мікрогемодинаміки: дилатація судин, стаз крові, сладж еритроцитів та утворення мікротромбів. Безпосередньо під стоншеними ділянками епідермісу мали місце осередки свіжих крововиливів із тенденцією до злиття.
Описані зміни поширювалися і на м’язову тканину. Мікроскопічне дослідження скелетних м’язів в осередку гнійного запалення показало, що значна частина волокон некротизована, фрагментується і розпадається на грудочки. Ендота перимізій різко розрихлені набряком, інфільтровані численними полінуклеарами. Нерідко виявлялися мікроабсцеси, ділянки геморагічної інфільтрації. Однак зрідка зустрічалися поодинокі гігантські клітини з гіперхромними ядрами як ознака регенераторного процесу в м’язах. У судинному руслі переважало артеріально-венозне повнокров’я з тромбозом. Такі зміни розвивалися на тлі морфологічних проявів мікроангіопатії, тому зазвичай поєднувалися із склеротично-запальними змінами дрібних судин артеріального і венозного типів.
На тлі зазначених змін, зокрема на краях ран, візуалізувалися осередки проліферації фібробластів та клітин ендотеліального типу. В базальних шарах збереженого епідермісу виявлялися ознаки проліферації камбіальних епітеліальних клітин. Аналогічні зміни спостерігали і на 5 день лікування.
На 10 добу ексудативно-деструктивні прояви зберігалися із слабовираженою тенденцією до згасання. На цьому терміні запальний інфільтрат складався переважно із полінуклеарних лейкоцитів та макрофагів, поширювався на всю товщу дерми, проникаючи в субдермальні ділянки та м’язову тканину. Подекуди спостерігали абсцедування. Мікроциркуляторні розлади у вигляді повнокров’я дилатованих судин, стазу та мікротромбозу були характерними для цього періоду. Гемодинамічні порушення підтримували набряк дерми та розшаровуючи її, але в меншому ступені. Поверхня зрізу, як правило, вкрита щільними лейкоцитарно-некротичними і фібриновими масами.
У дні та на краях ран визначалося формування грануляційної тканини (рис. 2). Екстрацелюлярний матрикс мав вигляд аморфної речовини та розміщених у ній фібробластів, макрофагів, нейтрофілів, лімфоцитів та новоутворених капілярів. Судини дилатовані та повнокровні з явищами крайового лейкостазу та тромбозу. Набряк дещо менший, але клітинний компонент суттєво переважав над волокнистим. При цьому значну його частку складали лейкоцити. В краях ран ознаки епітелізації були більш інтенсивними порівняно із попереднім терміном. Поверхня грануляційної тканини була вкрита фібриновими масами.
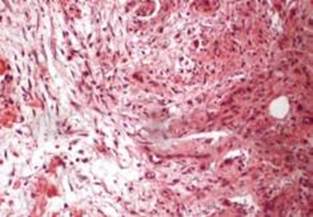
Рис. 2. Гістологічна картина м’яких тканин ранового дефекту хворого групи порівняння на 10 добу спостереження. Рання стадія формування грануляційної тканини — аморфна основна речовина, фібробласти, макрофаги та полінуклеари. Капіляри тонкостінні у невеликій кількості. Забарвлення гематоксиліном та еозином. х200.
У цей період спостереження найбільш яскраво проявлялася гетерогенність та нерівномірна динаміка мікроскопічних змін. Нерідко в грануляційній тканині виявлялися деструктивні явища та абсцедування. У прилеглих тканинах зберігалися виражені гемодинамічні розлади та запальна інфільтрація.
Гістологічне дослідження тканин рани на 15 добу показало зменшення кількості аморфної речовини та зростання числа клітинних елементів, серед яких переважали фібробласти. Колагенові волокна формували тонкопетлисту сітку фіброзної тканини, зливаючись місцями у більш потужні пучки та витісняючи клітинні елементи. Проте основний тканинний компонент у цей період складали численні капіляри із муфтоподібним потовщенням стінок та повнокровними просвітами. Облітеровані судини майже не візуалізувалися.
У міжсудинних проміжках зберігалася запальна інфільтрація, нерівномірний набряк тканини. Нерідко виявлялися осередкові скупчення полінуклеарів та дрібні абсцеси.
Мікроскопічний аналіз тканин ранового дефекту у хворих, яким проводили вакуумну терапію, показав якісно інші тенденції у динаміці ранового процесу.
На 3-ю добу спостереження ми відмітили морфологічні прояви, аналогічні групі порівняння. В цьому періоді також головною ознакою були ексудативно-запальні, деструктивно-некротичні зміни та виражені розлади кровообігу. Хоча їх прояви були дещо меншими.
У поверхневих та глибоких шарах дерми, підшкірній клітковині та м’язовому шарах превалювали зміни, зумовлені реакцією судинного русла. Т ак, у судинах різного калібру мало місце повнокров’я дилатованих судин із стазом крові, сладжем еритроцитів та тромбоутворенням. Такі порушення супроводжувалися геморагіями, випаданням фібрину та набряком, найбільше вираженими в маргінальних зонах рани. Розширені лімфатичні судини містили полінуклеарні лейкоцити. Поряд спостерігали дистрофічні, некробіотичні та некротичні зміни волокнистих структур дерми.
Запальний інфільтрат охоплював усі шари та поширювався на гіподерму та м’язи, проникаючи у перита ендомізій. У складі інфільтрату переважали полінуклеарні лейкоцити, макрофаги і лімфоцити. Слід зазначити, що альтеративних змін зазнавали переважно крайові епітеліальні структури, колагенові та еластичні волокна. Разом з тим, зберігався відносно високий об'єм судин. На судинні стінки також поширювався запальний процес із розвитком ендота панваскуліту.
Суттєві зміни в динаміці гострого ранового процесу починали виявлятися з 5-ї доби. Так, зменшувалася інтенсивність запальної реакції, в складі інфільтрату починали переважати лімфоцити та макрофаги. З’являлися поодинокі гігантські багатоядерні клітини. Тканинний детрит резорбувався. На тлі облітерованих капілярів виявлялися розсипні тяжі з ендотеліоподібних клітин із гетерохромними ядрами. Довкола тяжистих структур відмічався початок формування молодих колагенових волокон. Частина капілярів із звуженим просвітом з проліферацією периваскулярних елементів. Така морфологічна структура тканин характеризувала початок формування здорової грануляційної тканини. Поряд з цим суттєво знижувався набряк тканин і починав формуватися екстрацелюлярний матрикс. Це морфологічно свідчило про перехід ранового процесу з фази запалення у фазу проліферації.
На 10 добу використання вакуумної терапії спостерігали виражену фібропластичну реакцію. Хоча незначна частина судин мікроциркуляторного русла перебувала в дилатованому стані, інші, в глибоких, поверхневих сплетеннях і в краях рани мали всі ознаки регенерації. У гіподермі та в ділянці фасцій спостерігали проліферацію ендотелію, який формував вертикальні трубчасті структури у напрямку ранової поверхні. Тут же активно проліферували фібробласти. В краях рани також мали місце подібні зміни, проте їхнє поширення було направлене паралельно рановій поверхні. Формувався масив грануляційної тканини з високою щільністю тонкостінних судин та переважною інфільтрацією лейкоцитами та лімфоцитами.
Волокнисті структури в цей період майже не візуалізувалися або були представлені тонкопетлистою сіткою з великою кількістю клітин гістіоцитарного та гематогенного походження. У краях рани спостерігали ознаки проліферації базальних шарів епідермісу.
Загалом морфологічна картина грануляційної тканини на цьому терміні відповідала змінам, які ми спостерігали у хворих групи порівняння на 15 добу лікування (рис. 3).
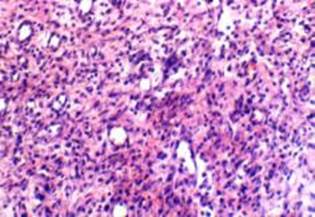
Рис. 3. Гістологічна картина м’яких тканин ранового дефекту хворого основної групи на 10-ту добу вакуумної терапії. Молода грануляційна тканина. Переважає поліморфноклітинний інфільтрат на тлі достатньо густої сітки колагенових волокон. Забарвлення гематоксиліном та еозином. *200.
У пацієнтів основної групи через 15 діб спостереження морфологічно відмічається сформована грануляційна тканина.
У біоптатах краю ран спостерігали добре виражені ознаки епітелізації. Аморфний міжклітинний матрикс майже повністю заміщений волокнистою сполучною тканиною. Волокнистий компонент візуально переважав над клітинним. Кількість судин також зменшувалася. Частина капілярів облітерувалася, периваскулярна строма ущільнювалася. стаз, аглютинація еритроцитів та мікротромбози виявлялися зрідка, що свідчило про суттєве поліпшення гемодинаміки. Як наслідок, набряк в дермі, гіподермі та підлеглій м’язовій тканині був слабовиражений.
Клітинна інфільтрація ставала нерівномірною і змінювала свій склад. Кількість полінуклеарів зменшувалася, натомість збільшувалася популяція гістіоцитів та лімфоцитів. З’являлися ділянки дозріваючої та добре васкуляризованої сполучної тканини.
Це свідчило про перехід ранового процесу в третю фазу — епітелізації та формування рубця.
Підсумовуючи результати порівняльного морфологічного дослідження ран у хворих із синдромом діабетичної стопи, можна стверджувати, що вакуумна терапія значно поліпшує мікрогемодинаміку ран, зменшує прояви запальних та деструктивних змін, пришвидшує організацію екстрацелюлярного матриксу, оптимізуючи таким чином регенераторний процес та формування якісної грануляційної тканини. Це дозволяє поліпшити перебіг ранового процесу, стимулювати процеси регенерації та скоротити терміни підготовки рани до пластичного закриття в середньому на 5 днів.
Перспективи подальших досліджень: вивчення динаміки морфологічних змін тканин при різних режимах вакуумної терапії у хворих із різними патогенетичними формами синдрому діабетичної стопи, з метою оптимізації схем диференційованого лікування вищезазначених пацієнтів.
мікроциркуляція вакуумний рана регенерація.
Список літератури
- 1. Абаев Ю. К. Раны и раневая инфекция: справочник хирурга / Ю. К. Абаев // Ростов на Дону: Феникс, 2006. — 427 с.
- 2. Синдром диабетической стопы в клинической практике / В. Н. Оболенский, Т. В. Семенова, П. Ш. Леваль, А. А. Плотников // Русский мед. журнал. — 2010. — № 2. — С. 45−58.
- 3. Удовиченко О. В. Диабетическая стопа / О. В. Удовиченко, Н. М. Грекова. — М.: Практическая медицина, 2010. — 272 с.
- 4. Храмилин В. Н. Современные аспекты местного лечения хронических ран нижних конечностей у больных сахарным диабетом / В. Н. Храмилин // Сахарный диабет. — 2005. — № 4. — С. 1−8.
- 5. Кривощеков Е. П. Роль вакуум-терапии в комплексном лечении осложненных форм диабетической стопы / Е. П. Кривощеков, Е. Б. Ельшин // Известия Самарского научного центра Российской академии наук. — 2014. — Т. 16, № 5(4). — С. 1286−1288.
- 6. Комплексне лікування нейроішемічної форми синдрому діабетичної стопи: можливості вакуум-терапії / В.І. Русин, В. В. Корсак, В. В. Русин [та ін.] // Шпитальна хірургія. — 2014. — № 3. — С. 51−53.
- 7. Consensus statement on negative pressure wound therapy for the management of diabetic foot wounds / G. Andros, D.G. Armstrong, В. Attinger [et al.] // Vasc. Dis. Manage. — 2006. — Suppl. — P. 1−32.
- 8. Клітинні перетворення в ранах у хворих із синдромом діабетичної стопи на фоні вакуум-терапії / О.М. Бєсєдін, К. В. Циганков, І.В. Кужевський, П. О. Гриценко // Морфологія. — 2015. — Т. 9, № 2. — С. 18−23.
- 9. Влияние терапии отрицательным давлением на репаративные процессы в мягких тканях нижних конечностей у пациентов с нейропатической и нейроишемической формами синдрома диабетической стопы / Е. Л. Зайцева, Л. П. Доронина [и др.] // Сахарный диабет. — 2014. — № 3. — С. 113−121.